Функциональные запоры римские критерии 4 2016
Функциональные нарушения моторики органов пищеварения в отличие от таковых, обусловленных структурными (органическими) изменениями со стороны того или иного органа, связаны с нарушениями его нервной и/или гуморальной регуляции. В основе развития таких заболеваний, включая и запоры функционального происхождения (ЗФП), лежит расстройство так называемой «оси мозг–кишка», дисрегуляция желудочно-кишечного тракта (ЖКТ) со стороны центральной нервной системы (ЦНС). Различные психоэмоциональные и социальные факторы, таким образом, влияют на функциональное состояние органов пищеварения, в частности, на их моторику, ускоряя или замедляя ее. С другой стороны, в этих условиях нарушается также реакция ЦНС на восходящие потоки, исходящие от ЖКТ, что приводит к неадекватному ее ответу. Выявлены также нарушения, наблюдающиеся на уровне самого ЖКТ, в т. ч. со стороны энтеральной нервной системы и рецепторного аппарата, на состояние которых влияет внутренняя среда в просвете ЖКТ, кишечная микрофлора, состояние проницаемости эпителиального барьера и многие другие факторы.
Все перечисленные аспекты объединяет так называемая биопсихосоциальная модель функциональных нарушений органов пищеварения, согласно которой симптомы развиваются из-за комбинации нескольких известных физиологических детерминант: нарушение моторики, висцеральная гиперчувствительность, изменение мукозального иммунитета и воспалительного потенциала, включающих в себя изменения в бактериальный флоре, а также изменения регулирования оси центральная нервная система — энтеральная нервная система как находящейся под влиянием психологических и социокультурных факторов [1].
В свете современных представлений о функциональных нарушениях органов пищеварения они определяются как устойчивые комплексы гастроинтестинальных симптомов, развивающиеся из-за комбинации нарушений моторики, висцеральной чувствительности и мукозального гомеостаза в определенных социально-средовых условиях и/или при наличии психологических личностных особенностей, семейной предрасположенности [1].
На протяжении последних десятилетий специалисты всех стран мира объединяют свои усилия для систематизации и углубления представлений о данной группе заболеваний с целью выработки единой классификации, общих принципов диагностики и лечения. Так, в 1990 г. был разработан первый консенсус по функциональным нарушениям органов пищеварения, получивший название Римский консенсус (Римские критерии). В 2016 г. состоялся очередной, четвертый, пересмотр данного консенсуса, пришедший на смену Римских критериев III (2006). Следует отметить, что внесенные изменения имеют в большей степени уточняющий характер, а многие принципиальные положения остались прежними. Как и в Римских критериях III, педиатрическим аспектам отведено два раздела классификации (G и H), разделяющих две возрастные группы: G. Функциональные нарушения у детей от рождения до 4 лет, H. Функциональные нарушения у детей старше 4 лет. ЗФП в рамках Римского консенсуса представлены синдромом раздраженного кишечника (СРК) и функциональными запорами (ФЗ). Также определенное отношение к данной проблеме имеют детская дисхезия и неретенционное недержание кала.
Ниже представлены соответствующие разделы классификации функциональных нарушений органов пищеварения в рамках Римских критериев III и IV, в т. ч. и касающиеся взрослых больных, сопровождающихся запорами (табл. 1).
Заболевания, обозначенные в Римских критериях, не всегда совпадают с нозологическими единицами, выделенными Международной классификацией болезней, руководствоваться которой приходится в повседневной практике для кодирования диагноза. Ниже представлены коды болезней с ЗФП по МКБ-10.
КОДЫ МКБ-10
- К 58. Синдром раздраженного кишечника (СРК)
- К 58.0. СРК с диареей
- К 58.9. СРК без диареи
- К 59.0. Запор
- К 59.1. Функциональная диарея
- К 59.2. Неврогенная возбудимость кишечника, не классифицируемая в других рубриках
- К 59.8. Другие уточненные функциональные нарушения кишечника
- К 59.9. Функциональные нарушения кишечника неуточненные
Диагностические критерии заболеваний и состояний, связанных с запорами функционального происхождения, в соответствии с Римскими критериями IV (2016) приведены в табл. 2.
СРК, как следует из приведенного консенсуса, может быть диагностирован только у детей старше 4 лет. Согласно определению, под СРК понимают функциональные нарушения моторики ЖКТ в виде запора и/или диареи, сопровождающиеся болями в животе. В предыдущей редакции консенсуса принципиальное отличие понятия ФЗ от понятия СРК заключалось в отсутствии болевого синдрома у пациента с ЗФП. Трактовка различий СРК и ФЗ сохранилась в Римских критериях IV в разделе, посвященном нарушениям кишечной моторики у взрослых пациентов. Кроме того, в последнем консенсусе указано, что боли при СРК так или иначе связаны с дефекацией. В Римских критериях III формулировка была более категоричная: «боли проходят после дефекации». Диагностические критерии СРК в Римских критериях III для взрослых и для детей были аналогичные, но изменились в последней редакции.
Боли в животе по Римским критериям IV являются не только признаком СРК, но и не противоречат диагнозу ФЗ. Это изменение обусловлено тем обстоятельством, что по данным проведенных исследований у 75% детей различных возрастов с запорами наблюдаются боли в животе [6]. Более того, в критериях 2016 г. подчеркивается, что при СРК с запорами боли не проходят с разрешением самого запора и детям, у которых после дефекации боли проходят, следует ставить диагноз ФЗ, но не СРК. Что касается ФЗ, то ведущим симптомом в этом случае является запор, а боли в животе (и вздутие живота) хотя и могут присутствовать в клинической картине, все-таки являются симптомами второго плана.
Следует обратить внимание и на временные аспекты. Диагноз СРК может быть поставлен, если боли в животе в сочетании с запором наблюдаются по крайней мере 4 дня в месяц по крайней мере в течение 2 месяцев до установления диагноза. В случае ФЗ признаки должны наблюдаться по крайней мере 1 раз в неделю как минимум в течение 1 месяца [4, 5, 7].
Также следует обратить внимание на так называемые симптомы «тревоги», которые исключают диагноз ЗФП [4, 5]:
- раннее начало запора (в возрасте < 1 мес жизни);
- выделение мекония более чем через 48 ч после рождения у доношенного новорожденного;
- семейный анамнез в отношении болезни Гиршпрунга;
- лентовидный стул;
- кровь в стуле при отсутствии анальных трещин;
- задержка развития;
- лихорадка;
- рвота желчью;
- аномалия щитовидной железы;
- выраженное вздутие живота;
- перианальная фистула;
- аномальное положение ануса;
- анальный рефлекс или кремастерный рефлекс отсутствуют;
- снижение мышечной силы нижних конечностей/тонуса/рефлексов;
- пучок волос над остистым отростком позвонка (косвенный признак spina bifida);
- впадина в области крестца (косвенный признак spina bifida);
- отклонение межъягодичной борозды;
- сильный страх во время осмотра ануса;
- рубцы в области анального отверстия.
Основная цель при лечении ЗФП — обеспечение регулярной безболезненной дефекации стулом мягкой консистенции, а также предотвращение скопления каловых масс.
Этого возможно добиться в результате проведения комплекса мероприятий: обучения родителей и ребенка, коррекции поведения, ежедневного приема слабительных препаратов и изменения режима питания. Необходимо подчеркнуть, что лечение ЗФП следует проводить дифференцированно с учетом возраста ребенка и стадии ЗФП: компенсированной, субкомпенсированной и декомпенсированной.
Первый этап лечения ЗФП — разъяснительная работа с родителями и детьми (старшего возраста), когда объясняются возможные причины и механизмы возникновения запоров. Иногда ЗФП могут быть обусловлены особенностями внутрисемейной обстановки или усугубляться ими, так что может понадобиться помощь семейного психолога.
Поведенческая терапия основывается на выработке режима посещения туалета с целью добиться регулярной дефекации. Обязательное условие эффективной дефекации — обеспечить хороший упор для ног, что может быть обеспечено наличием в туалете низкой скамейки для ребенка, на которую он может поставить ноги. Если дефекация не удалась, ребенка ни в коем случае нельзя наказывать, и, наоборот, нужно хвалить в случае удачи [8].
Коррекция питания при запорах является обязательным компонентом лечения: показана диета, включающая зерновые, фрукты и овощи [9]. Недостаточное употребление пищевых волокон в ежедневном рационе является фактором риска возникновения запора [8]. Национальной академией наук США (United States National Academy of Sciences) предложена норма потребления пищевых волокон из расчета 14 г на 1000 ккал (15 г для годовалого ребенка в сутки), комитетом по питанию Американской академии педиатрии (American Academy of Pediatrics, AAP) — 0,5 г/кг (до 35 г/сут) [10–12]. Российское общество детских гастроэнтерологов рекомендует следующий расчет нормы потребления пищевых волокон: к возрасту ребенка прибавить 5–10 г в сутки ((5–10) + n, где n — возраст в годах, т. е. 6–11 г/сут для годовалого ребенка) [13]. Из питания рекомендуется исключить продукты, задерживающие опорожнение кишечника (табл. 3). Не рекомендуется «пища-размазня», пюреобразная, «еда на ходу», «перекусы». Наоборот, показана рассыпчатая пища, мясо/птица/рыба «куском». Обязателен «объемный» завтрак — для стимуляции «гастроцекального рефлекса».
При употреблении в пищу грубой клетчатки необходимо обеспечить достаточное потребление воды. Только одновременное употребление 25 г растительной клетчатки и не менее 2 л жидкости в сутки ускоряет кишечный транзит и размягчает кал [14].
Лекарственная (поддерживающая) терапии
Безболезненный стул мягкой консистенции достигается с помощью слабительных средств. При выработке тактики лечения ФЗ крайне важна индивидуальная программа лечения с учетом преморбидного фона и сопутствующей патологии. Главной проблемой в лечении ФЗ у детей являются возрастные ограничения при применении слабительных средств. Наряду со слабительными средствами, эффективно назначение нормокинетиков (тримебутин), пре- и пробиотиков, а также у части больных спазмолитиков и желчегонных средств.
В отечественной практике из всех групп слабительных, применяемых в детской практике, предпочтение отдается препаратам, обладающим осмотическим эффектом. Основным механизмом их действия является размягчение стула за счет удержания воды, что облегчает транспортировку химуса и делает дефекацию менее затрудненной. При этом увеличивается объем стула, стимулируется моторика кишечника, нормализуется транзит. К средствам этой группы относятся препараты на основе лактулозы, лактитола, макрогола. Особенностью лактулозы и лактитола является их пребиотическое действие. В качестве дополнительных средств лечения ЗФП могут рассматриваться препараты спазмолитики растительного происхождения, обладающие влиянием на секрецию желудочного сока и перистальтику кишечника [9]. Клинический опыт лечения запоров свидетельствует о целесообразности использования в комплексной терапии запоров желчегонных средств. Общие принципы дифференцированной терапии ЗФП в зависимости от характера патологического процесса приведены в табл. 4.
Таким образом, запоры функционального происхождения, являясь распространенной патологией детского возраста, требуют к себе внимания и нередко кропотливой дифференциальной диагностики. Своевременная диагностика функциональных нарушений органов пищеварения и их лечение необходимы для предотвращения развития осложнений и их эволюции в патологию органическую.
Литература
- Drossman D. A. The functional gastrointestinal disorders and the Rome III process // Gastroenterology. 2006; 130: 1377–1390.
- Drossman D. D., Corazziari E., Delvaux M. et al. Rome III: The Functional Gastrointestinal Disorders. 3 rd Edition. VA, USA: Degnon Associates, Inc.; 2006.
- Drossman D. A., Hasler W. L. Rome IV — Functional GI Disorders: Disorders of Gut-Brain Interaction // Gastroenterology. 2016; 150 (6): 1257–1261.
- Hyams J. S., Di Lorenzo C., Saps M., Shulman R. J., Staiano A., van Tilburg M. Childhood Functional Gastrointestinal Disorders: Child // Adolescent. Gastroenterology. 2016; 150 (6): 1469–1480.
- Benninga S., Nurko M. A., Faure C., Hyman P. E., James Roberts I. St., Schechter N. L. Childhood Functional Gastrointestinal Disorders: Neonate/Toddler // Gastroenterology. 2016; 150 (6): 1443–1455.
- Burgers R., Levin A. D., Di Lorenzo C. et al. Functional defecation disorders in children: comparing the Rome II with the Rome III criteria // J Pediatr. 2012; 161: 615–620 e1.
- Lacy B. E., Mearin F., Chang L., Chey W. D., Lembo A. J., Simren M., Spiller R. Bowel Disorders // Gastroenterology. 2016; 150 (6): 1393–1407.
- Inan M., Aydiner C., Tokuc B. Factors associated with childhood constipation // J Paediatr Child Health. 2007; 43: 700–706.
- Rasquin A., Di Lorenzo C., Forbes D. Childhood functional gastrointestinal disorders: Child/adolescent // Gastroenterology. 2006; 130: 1527–1537.
- Morais M. B., Vitolo M. R., Aguirre A. N., Fagundes-Neto U. Measurement of low dietary fiber intake as a risk factor for chronic constipation in children // J Pediatr Gastroenterol Nutr. 1999; 29: 132–135.
- Lee W. T., Ip K. S., Chan J. S., Lui N. W., Young B. W. Increased prevalence of constipation in pre-school children is attributable to under-consumption of plant foods: A community-based study // J Pediatr Child Health. 2008; 44: 170–175.
- Castillejo G., Bulló M., Anguera A., Escribano J., Salas-Salvadó J. A controlled, randomized, double-blind trial to evaluate the effect of a supplement of cocoa husk that is rich in dietary fiber on colonic transit in constipated pediatric patients // Pediatrics. 2006 Sep; 118 (3): e641–8.
- Хавкин А. И., Файзуллина Р. А., Бельмер С. В., Горелов А. В., Захарова И. Н., Звягин А. А., Корниенко Е. А., Нижевич А. А., Печкуров Д. В., Потапов А. С., Приворотский В. Ф., Рычкова С. В., Шеина О. П. Диагностика и тактика ведения детей с функциональными запорами (Рекомендации общества детских гастроэнтерологов) // Вопросы детской диетологии. 2014; 12 (4): 49–63.
- Carbohydrate and dietary fiber. In: Kleinman R. E., ed. Pediatric Nutrition Handbook, 6 th Edition, Community on Nutrition. American Academy of Pediatrics 2009; 104.
С. В. Бельмер*, 1, доктор медицинских наук, профессор
А. И. Хавкин*, доктор медицинских наук, профессор
Д. В. Печкуров**, доктор медицинских наук, профессор
* ФГБОУ ВО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
** ФГБОУ ВО СамГМУ МЗ РФ, Самара
1 Контактная информация: belmersv@mail.ru
Купить номер с этой статьей в pdf
Источник
В статье подробно рассмотрены Римские критерии IV и приведен алгоритм ведения пациентов с синдромом раздраженного кишечника
Введение
Функциональные заболевания кишечника (ФЗК) очень широко распространены во всем мире. Эти расстройства затрагивают все слои общества, независимо от пола, возраста, расы, вероисповедания, цвета кожи или социально-экономического статуса. В 2016 г. были опубликованы Римские критерии IV [1], надежды на которые, к сожалению, не вполне оправдались, т. к. гастроэнтерологи-интернисты так и не получили универсальные инструменты для курации «функциональных» пациентов. В то же время обновленные критерии представляют собой не прекращающие адаптироваться клинические рекомендации, определяющие вектор клинического мышления как в случаях постановки диагноза, так и в случаях выбора методов терапии.
В отличие от предыдущей классификации, в разделе функциональных заболеваний кишечника появилась новая форма – «опиоид-индуцированный запор», призванная обратить внимание клиницистов на резко возросшую частоту применения опиатов и связанное с этим большое количество побочных эффектов. Эта форма не рассматривается как отдельное заболевание, а классифицируется как опиоид-индуцированное неблагоприятное последствие.
Римские критерии IV. Раздел С. Функциональные расстройства кишечника:
C1. Синдром раздраженного кишечника.
C2. Функциональный запор.
C3. Функциональная диарея.
С4. Функциональное вздутие.
C5. Неспецифическое функциональное кишечное расстройство.
С6. Опиоид-индуцированный запор.
Определение и эпидемиология
Сегодня синдром раздраженного кишечника (СРК) – это рецидивирующее функциональное расстройство ЖКТ, главным симптомом которого является боль в животе в непременной ассоциации с изменением кишечной функции, проявляющимся преобладанием либо диареи (СРК-Д), либо запоров (СРК-З) или их чередованием (СРК-С, смешанный вариант). Диагноз СРК остается исключительно клиническим. Сложность изучения СРК, особенно с позиций его эпидемиологии, заключается в отсутствии до сих пор универсального и специфичного биологического маркера.
Согласно метаанализу, опубликованному в 2012 г., в который по довольно строгим критериям отбора вошло 80 клинических исследований (с общим числом пациентов 260 960), распространенность СРК в мире составляет 11,2% (95% ДИ: 9,8–12,8%) [2]. Заболеваемость оценивается как 1,35–1,5%, о чем свидетельствуют 2 отдельных популяционных исследования длительностью 10 и 12 лет [3, 4]. Встречаемость СРК среди женщин остается более высокой, чем среди мужчин. Молодые люди более подвержены развитию заболевания, нежели лица старше 50 лет. Любой случай манифестации клинической картины СРК у пациентов старшей возрастной категории должен настораживать интерниста в отношении исключения органической патологии.
Этиопатогенез СРК очень сложен и до сих пор до конца не изучен. На заре изучения этой проблемы из публикаций мы знали о феномене висцеральной гиперчувствительности, который объяснялся нарушением моторики ЖКТ, с безуспешными попытками увязать особенности этого нарушения с каким-либо вариантом СРК, и недостаточными на тот момент знаниями о нарушениях по оси «головной мозг – ЖКТ». Сегодня среди звеньев этиопатогенеза синдрома как наиболее актуальные рассматриваются социально-экономический статус, генетическая предрасположенность, возможность формирования заболевания у ребенка родителями, страдающими СРК, психологические аспекты, висцеральная гиперчувствительность, нарушения моторики ЖКТ, изменения в нейроэндокринной системе (ось «головной мозг – ЖКТ»), low-grade воспаление, концепция постинфекционного СРК, дисбаланс микробиоты и, наконец, факторы питания [5]. В концепции формирования заболевания в каждом конкретном случае, очевидно, имеет значение несколько этиологических факторов, запускающих несколько патофизиологических механизмов (рис. 1). И сложность курации подобных больных заключается в том, что в каждом конкретном случае сочетание этиопатогенетических механизмов индивидуально [6]. 
Принимая во внимание многокомпонентность причин и механизмов формирования СРК, необходимо отметить, что все эти звенья играют такую же роль и при других функциональных заболеваниях ЖКТ. Факт возможности перекреста функциональной патологии у одного и того же больного сегодня безоговорочно принят Римским соглашением, а наиболее частым «соседом» СРК в этом перекресте является функциональная диспепсия [7, 8]. Это, в свою очередь, существенно усложняет курацию пациентов, приводит к назначению врачами большого количества порой ненужных препаратов и объясняет низкий уровень приверженности пациентов проводимому лечению. Все это крайне важно учитывать при лечении так называемых «функциональных» больных.
Концепция Римских диагностических критериев IV и классификация СРК
Современные Римские диагностические критерии СРК IV [1] имеют ряд принципиально важных отличий от предыдущей редакции. Среди них – анамнез (начало клинических проявлений в течение не менее 6 мес. до постановки диагноза), текущая активность (наличие симптомов в течение последних 3 мес.), частота (указанные в критериях симптомы присутствуют не реже 1 раза в неделю, в отличие от 3 дней в месяц, как предлагалось в Римских критериях III), и все это – при отсутствии очевидных анатомических и физиологических отклонений при проведении рутинного клинического обследования по показаниям, иными словами, при отсутствии «симптомов тревоги».
Римские диагностические критерии СРК IV
Рецидивирующая абдоминальная боль в среднем как минимум 1 день в неделю за последние 3 мес., ассоциированная с 2 и более следующими симптомами:
– связанная с дефекацией;
– ассоциированная с изменением частоты стула;
– ассоциированная с изменением формы стула.
Критерии валидны при условии их наличия в течение последних 3 мес. с началом симптомов не менее 6 мес. назад!
Кроме того, в отличие от предыдущих редакций Римских критериев, из текущего определения исключен термин «дискомфорт» на том основании, что, во-первых, не все языки мира имеют в своем арсенале это слово, а во-вторых, и это, пожалуй, главное, – различная и неопределенная трактовка понятия «дискомфорт» пациентами часто приводит к ошибочному диагнозу. И этот последний факт был документально подтвержден в клиническом исследовании [9].
Таким образом, сегодня главный отличительный симптом СРК – это боль в животе, связанная с дефекацией, в неразрывной ассоциации с нарушением кишечной привычки, а не дискомфорт, вздутие, растяжение или какие-либо другие ощущения, которые могут встречаться у больных с другой функциональной патологией, например, при функциональном запоре или диарее. Эта концепция, отражающая современный взгляд на диагностику ФЗК, наглядно представлена на рисунке 2.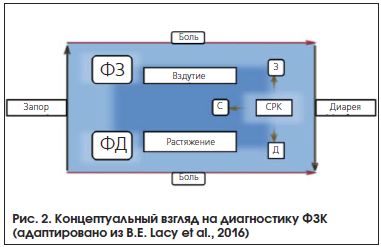
Еще одной отличительной чертой обновленных рекомендаций является замена фразы «облегчение после дефекации» на «связанную с дефекацией», т. к. мировой клинический опыт показывает, что у довольно значительной части больных этого облегчения не происходит, более того, ряд пациентов с СРК отмечают ухудшение после дефекации.
Мы полагаем, что все эти нюансы нового взгляда на СРК позволят существенно снизить количество ложных диагнозов и, наоборот, его гипердиагностики.
Принцип классификации СРК остался неизменным и основан на Бристольской шкале формы стула [10], типы 1 и 2 которой свидетельствуют о запоре, а типы 6 и 7 – о диарее. Более того, использование Бристольской шкалы формы стула позволит не только избежать диагностической ошибки, но и значительно сократить время приема пациента, что в современных условиях работы поликлинического врача является чрезвычайно полезным.
Таким образом, как это было и ранее, опираясь на описанную выше шкалу, принимая во внимание частоту встречаемости того или иного типа стула, врач устанавливает форму СРК. При этом надо помнить, что один и тот же пациент в ходе естественного течения своего заболевания может иметь различные варианты СРК.
Этапы диагностики и дифференциальная диагностика СРК
Как уже не раз говорилось, любая функциональная патология является диагнозом исключения. И когда жалобы и анамнез больного позволяют предположить, например, СРК, следующим обязательным этапом диагностики, равно как и в любом другом случае, является физикальный осмотр, который позволяет успокоить пациента и исключить или заподозрить органическую патологию.
Следующим шагом в диагностике СРК является выполнение лабораторных тестов и инструментального обследования, если таковые не проводились ранее или к ним есть определенные показания. Они включают в себя оценку клинического анализа крови, маркеров воспаления, в частности, С-реактивного белка крови, эндоскопическое исследование (колоноскопию) всем лицам старше 50 лет либо во всех случаях семейного анамнеза колоректального рака, имеющегося гематохезиса, подозрения на микроскопический колит. Кроме того, по показаниям необходимо выполнять серологическую диагностику целиакии у пациентов с преобладанием диареи и при смешанном варианте, особенно у тех, кто не ответил на инициированную эмпирическую терапию, оценивать маркеры функции щитовидной железы при клинических подозрениях на ее патологию; исключить инфекционную природу диареи, синдром мальабсорбции желчных кислот, панкреатическую недостаточность, Clostridium difficile-ассоциированную болезнь, провести дыхательные тесты и др.
Перечень нозологий, с которыми должна проводиться дифференциальная диагностика, и их особенностей представлен в наших предыдущих публикациях [11]. Следует отметить, что объем обследования больного СРК в итоге, безусловно, зависит от уровня профессионализма врача и должен быть регламентирован показаниями.
Лечение
Лечение больных СРК, даже с учетом обновленных клинических рекомендаций, остается очень сложной задачей. Это связано с многообразием факторов, приводящих к развитию заболевания, о чем говорилось выше, чрезвычайно сильной зависимостью рецидивирования заболевания от состояния психоэмоциональной сферы, наличием в большинстве случаев коморбидности и синдрома «перекреста».
В настоящее время в арсенале интерниста при курации пациента с СРК нет универсального инструмента, а именно препарата или комбинации препаратов, которые были бы эффективны в большинстве случаев хотя бы одного из вариантов заболевания.
Попытки разработать эффективную схему терапии СРК с пролонгированным действием до сих пор остаются безуспешными. Это связано еще и с тем, что проблема поиска и объективной оценки эффективности того или иного препарата очень непроста из-за чрезвычайно высокого эффекта плацебо у «функциональных» пациентов, который, по самым взвешенным оценкам, составляет от 25% до 59%, в среднем – 42% [12, 13].
Вот почему, согласно Римским рекомендациям IV, лекарственную терапию, так же как и в предыдущих редакциях, предлагается назначать по принципу преобладающего симптома (табл. 1).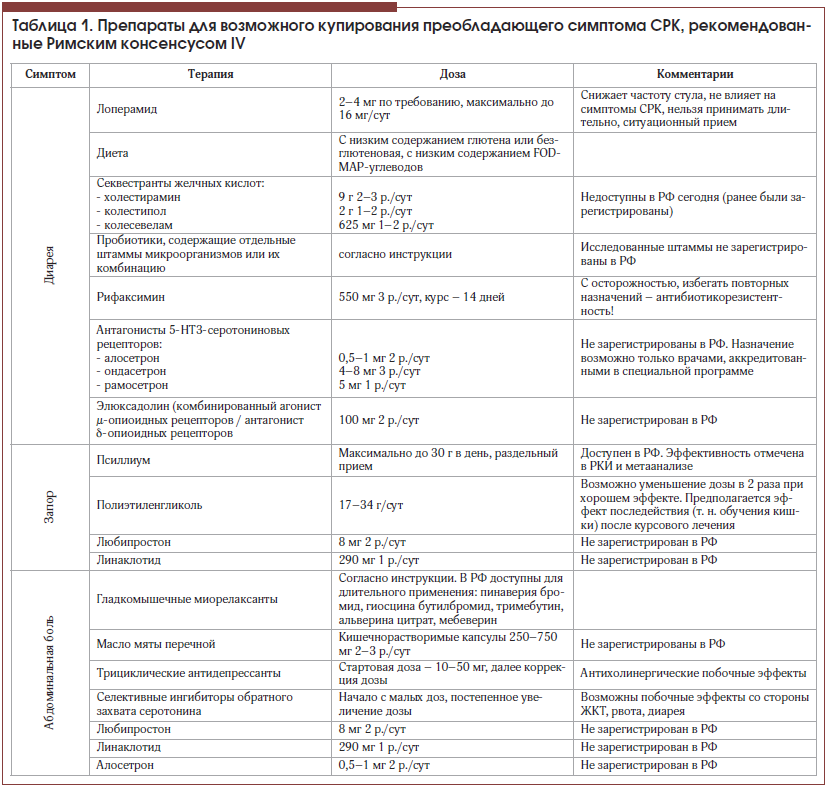
Несмотря на заметное прибавление лекарственных препаратов новых классов, очевидно, что, как и в прошлых версиях клинических рекомендаций, российский гастроэнтеролог располагает лишь 1/3 из предложенных препаратов ввиду отсутствия их регистрации в РФ. Вероятно, поэтому на фоне недобросовестной рекламы «препаратов для СРК» фармакотерапия таких пациентов в реальной практике приводит к необоснованной полипрагмазии. Так, среди назначаемых средств для лечения СРК можно обнаружить ферментные препараты, антациды, препараты, которые вообще трудно классифицировать, имеющие нераспознанный механизм действия, и многое другое.
В качестве так называемой базисной или приоритетной терапии СРК, направленной на борьбу с висцеральной гиперчувствительностью и, соответственно, с болью, свою актуальность сохранили спазмолитики с NNT 5 и трициклические антидепрессанты, также имеющие NNT 5 [14]. Далее в зависимости от варианта нарушения стула рассматривается назначение псиллиума, полиэтиленгликоля и других препаратов с целью нормализации стула, в ряде случаев с дополнительным положительным влиянием на боль.
Что касается появления в рекомендациях группы пробиотиков, то здесь имеется диссонанс. Дело в том, что практически ни один штамм, прошедший в западных странах научную оценку возможности применения при СРК, не зарегистрирован в РФ. И мы полагаем, что экстраполировать эффективность этих штаммов на все препараты с пробиотическими свойствами, представленными в российской аптечной сети, ошибочно.
В связи с таким многообразием указанных проблем необходимо отметить растущий интерес к изучению влияния на клинику СРК так называемой комплементарной медицины и, в частности, фитотерапии, прежде всего, с позиции доказательности [15].
Таким комбинированным фитопрепаратом является Иберогаст® (смесь экстрактов 9 растений), который изначально использовался в основном для лечения функциональной диспепсии в Германии [16]. Иберогаст® является одним из наиболее изученных фитопрепаратов и существует на европейском рынке уже более 30 лет. В его состав входят экстракты из иберийки горькой, дягиля лекарственного, расторопши пятнистой, тмина обыкновенного, чистотела майского, ромашки аптечной, солодки голой, мелиссы лекарственной и мяты перечной [17]. Важно отметить, что многоцелевой характер действия препарата Иберогаст® реализуется путем влияния на различные патогенетические аспекты СРК (спазмолитическое, прокинетическое действие, снижение газообразования, противовоспалительное (антиоксидантное) действие, увеличение секреции хлоридов в кишечнике и т. д.) за счет многокомпонентного состава.
Клинические свойства препарата Иберогаст® были изучены в Германии у 208 пациентов с СРК с различными вариантами течения синдрома в 4-недельном рандомизированном двойном слепом плацебо-контролируемом исследовании. Было продемонстрировано, что применение препарата значительно улучшало качество жизни пациентов с СРК и существенно влияло на болевой абдоминальный синдром, уменьшая его, при этом 94% пациентов отметили переносимость препарата Иберогаст® как «хорошую» или «очень хорошую», при отсутствии значимых в отношении безопасности изменений лабораторных параметров [18]. Этот клинический эффект был опосредован влиянием препарата Иберогаст® на серотониновые (5-HT3 и 5-HT4), мускариновые (М3) и опиоидные рецепторы ЖКТ [17].
Накопленный опыт применения препарата Иберогаст® в лечении СРК позволил включить его в новейшие российские клинические рекомендации «Синдром раздраженного кишечника» в качестве потенциальной дополнительной терапии для достижения курации всего спектра симптомов заболевания [19]. Подобные выводы были и в опубликованном в 2011 г. Кохрейновском метаанализе [20].
Таким образом, в нашем арсенале мы имеет еще один препарат, который может назначаться в зависимости от конкретной клинической ситуации и фенотипа больного как в качестве основной или первичной терапии, так и дополнительной, особенно в случаях сочетания СРК с функциональной диспепсией (рис. 3). Эта рекомендация поддерживается Российским экспертным советом во главе с академиком В.Т. Ивашкиным [21].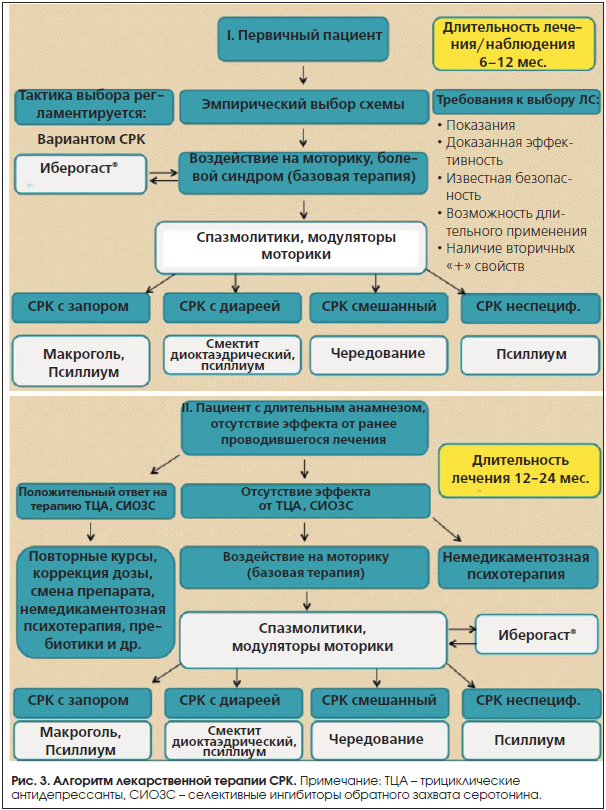
Источник


